Este é um artigo bastante interessante para quem deseja aprender como funcionam os carregadores de bateria. Trata-se de artigo bastante atua (2010) que merece ser lido pelos leitores que desejam saber mais sobre o princípio de funcionamento destes dispositivos presentes em todos os celulares, câmaras fotográficas, câmaras de vídeo e muito mais.
Os carregadores de baterias estão em toda parte. Dos Telefones celulares, câmeras fotográficas, laptops aos palmtops, Ipods, E-book readers que fazem uso de baterias recarregáveis todos precisam de um carregador. O princípio de funcionamento de um carregador de baterias é do que tratamos neste artigo destinado aos leitores que desejam se aprofundar no conhecimento desta tecnologia indispensável em nossos dias.
As pilhas, baterias ou células recarregáveis consistem em fontes de energia elétrica de origem química. Em outras palavras, uma reação química libera energia na forma de eletricidade, a qual é utilizada por um circuito externo. Para entender como funciona uma célula recarregável e portanto um carregador, vamos partir do princípio de funcionamento de uma pilha ou célula comum não recarregáveis. Podemos tomar como exemplo as pilhas secas ou as alcalinas.
Pilhas e Baterias Comuns (Não Recarregáveis)
Numa pilha ou bateria comum, existem dois eletrodos que fazem contato com uma substância química que possui um elevado potencial de reação, ou seja, dispõe de energia para liberar numa reação química. Esta substância é denominada eletrólito e tem as mais diversas composições, conforme o tipo de pilha ou bateria considerada. Para tornar as coisas mais simples, vamos tomar como exemplo uma pilha seca comum, que é vista em corte na figura 1.
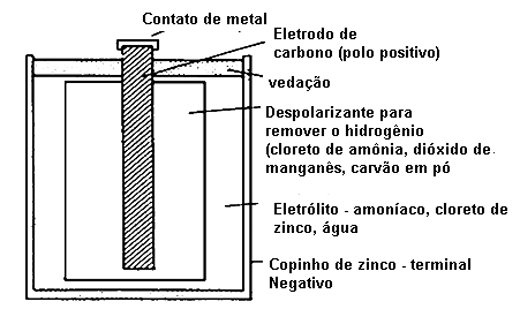
Nela, um dos eletrodos, o ligado ao pólo positivo consiste num bastão de grafite ou carvão e o outro consiste num "copinho" de zinco. A substância reagente ou eletrólito é uma mistura que contém manganês, amônia, e outras substâncias que têm finalidades as mais diversas, por exemplo, na estabilização da reação.
A substância reagente que seria o "combustível" da pilha, permanece inerte até o ponto em que um circuito externo seja ligado entre o pólo positivo e o pólo negativo da pilha "solicitando" assim a entrega de energia, conforme mostra a figura 2.
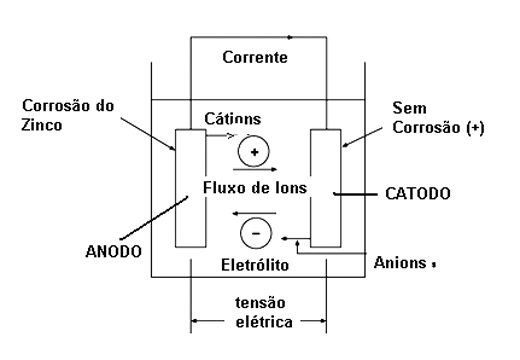
Quando a corrente é solicitada, a movimentação de cargas elétricas no circuito também passa a ocorre na forma de íons na substância e a reação química tem início. A substância começa então a reagir com o eletrodo negativo (copinho de zinco) de modo a liberar íons e com isso manter a corrente elétrica no circuito. O resultado é que nesta reação a substância se transforma entregando a energia de que dispõe e o copinho de zinco é consumido no processo.
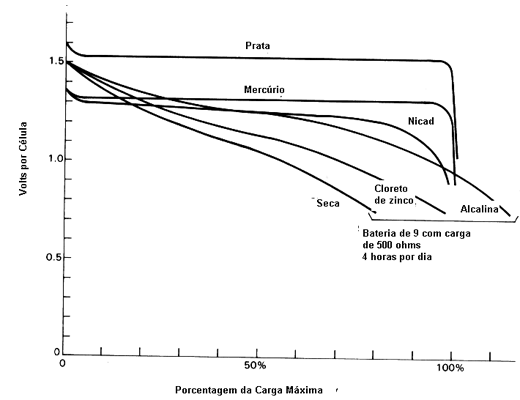
À medida que a pilha vai fornecendo sua energia, a substância do eletrólito vai se desgastando, o copinho de zinco consumido e com isso cada vez menos corrente vai se tornando disponível. Chega um determinado momento, em que a energia se reduz a tal ponto que a resistência interna da pilha aumenta e a corrente já não pode mais se fornecida ao circuito externo com a mesma intensidade. A tensão entre os pólos da pilha cai. A pilha está em sua fase final de esgotamento. A figura 3 mostra a curva típica de fornecimento de uma pilha seca comparada a de outros tipos.
Se examinarmos a pilha esgotada, veremos que a substância de seu interior se modificou e que um dos eletrodos se encontra corroído. Veja que as pilhas secas, possuem uma proteção adicional de papelão e aço sobre o copinho de zinco, justamente para evitar que a substância "vaze" quando a pilha se esgota. Essa substância é corrosiva, podendo afetar os aparelhos em que ela se encontrar, se o vazamento ocorrer.
É por esse motivo que se recomenda retirar as pilhas dos aparelhos que vão ficar muito tempo sem uso. Mesmo sem usar, a reação ainda ocorre de forma muito vagarosa, mas ao final de muito tempo, uma pilha deixada num aparelho, se esgota e pode vazar...
Pilhas comuns não são recarregáveis
Nas pilhas comuns (alcalinas, secas e outras) a reação que ocorre quando a energia é fornecida é irreversível, ou seja, "não tem volta". Uma vez que a substância reagente entregue a energia.
Em alguns casos, aquecendo um pouco a pilha ou ainda deixando-a em repouso pode-se reativar o restante da substância que ainda pode reagir e assim prolongar a vida útil da pilha. A idéia de que colocar as pilhas na geladeira, adotada por muitos, não é válida, pois o que faz a pilha reativar um pouco não é o frio mas sim o repouso...